Phát hiện thấy 26 bài viết liên quan đến chủ đề bảng hóa trị lớp 8.






























![[ HÓA HỌC 8-9] CÁCH NHỚ HÓA TRỊ NGUYÊN TỐ HÓA HỌC [ HÓA HỌC 8-9] CÁCH NHỚ HÓA TRỊ NGUYÊN TỐ HÓA HỌC](https://i.ytimg.com/vi/VIX7X0umeNY/hqdefault.jpg)
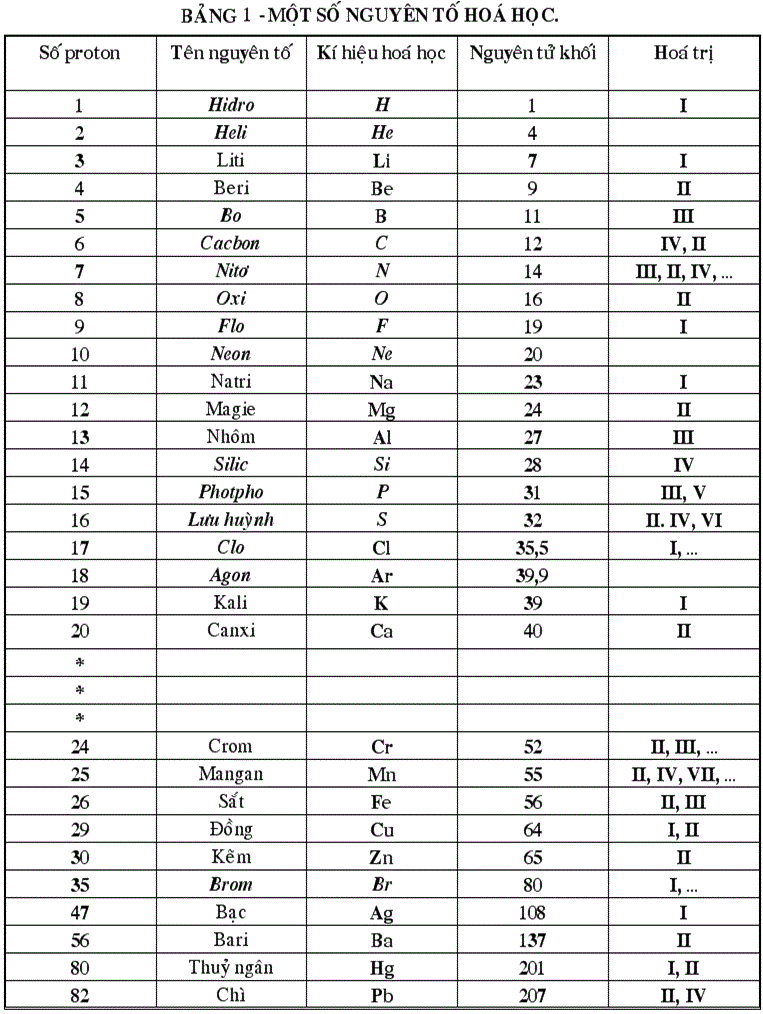
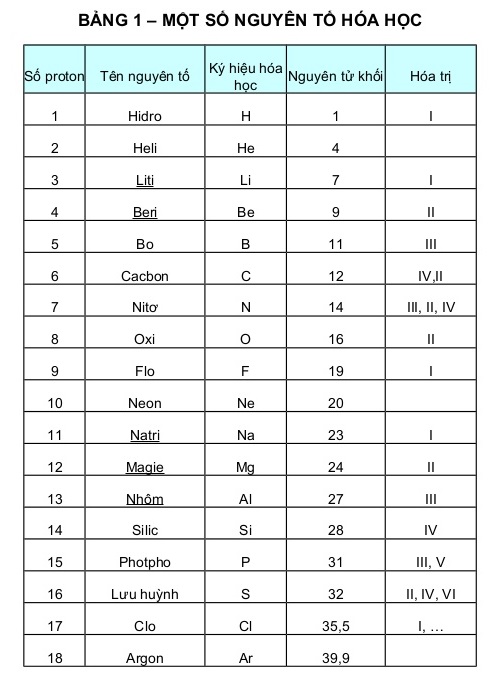
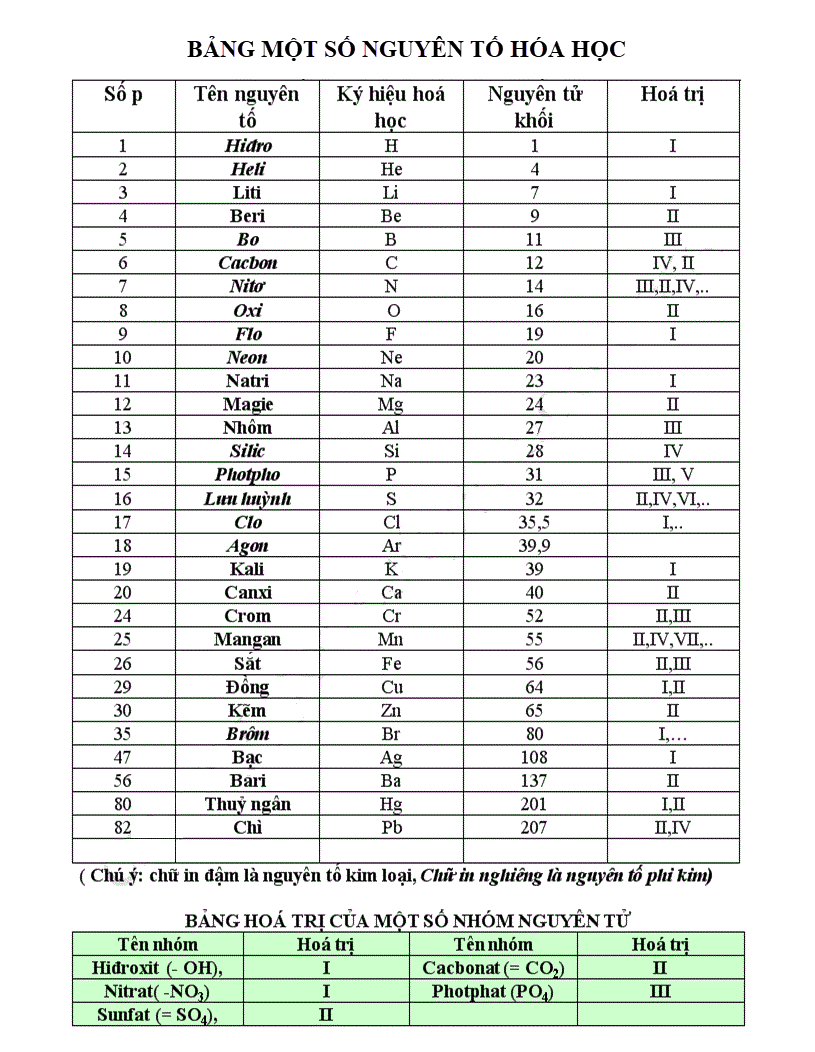
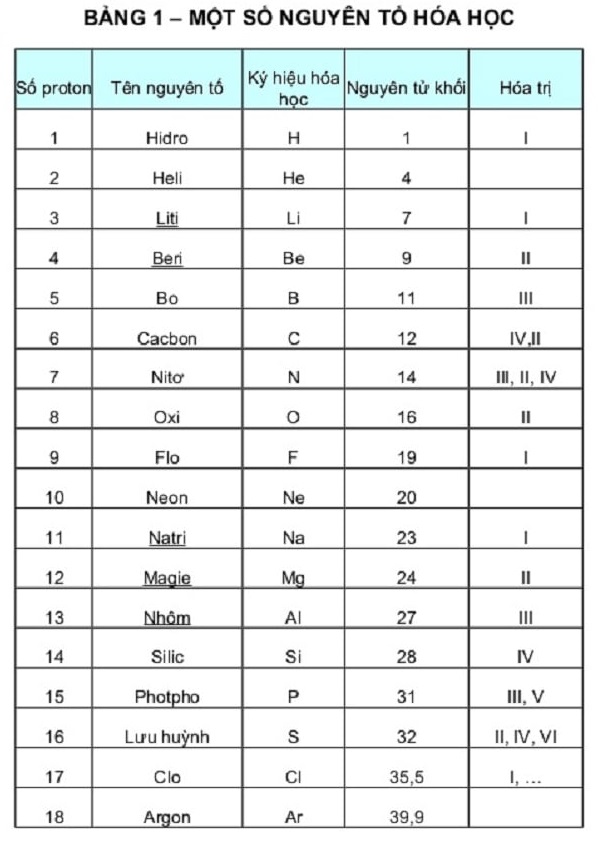
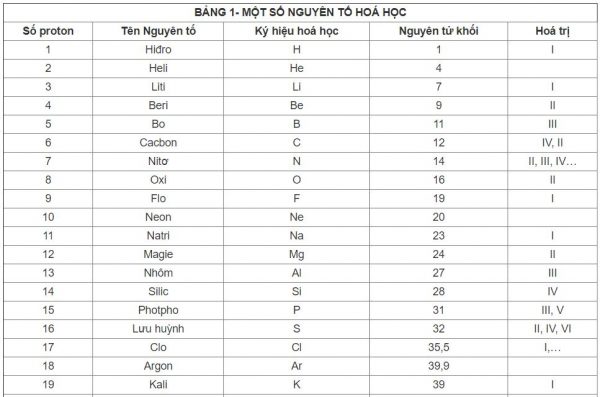
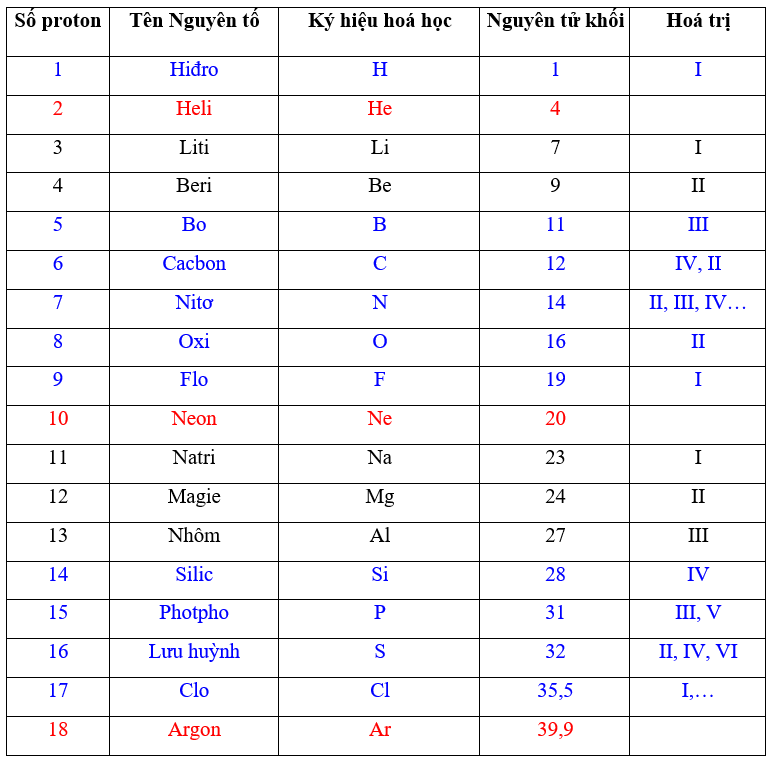
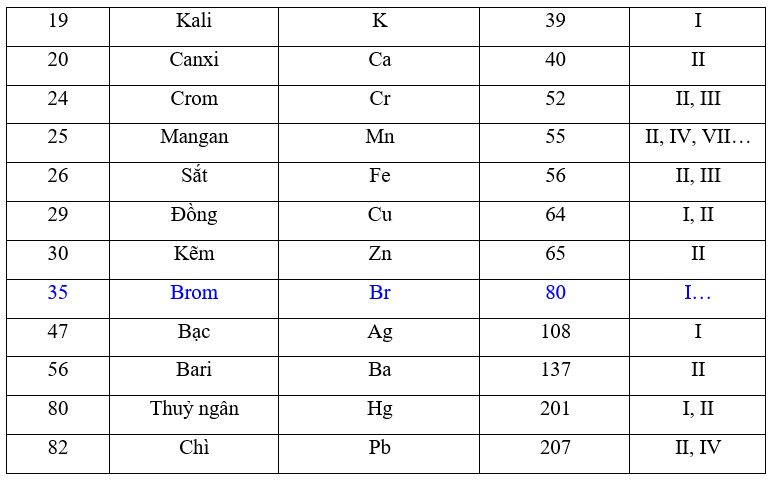
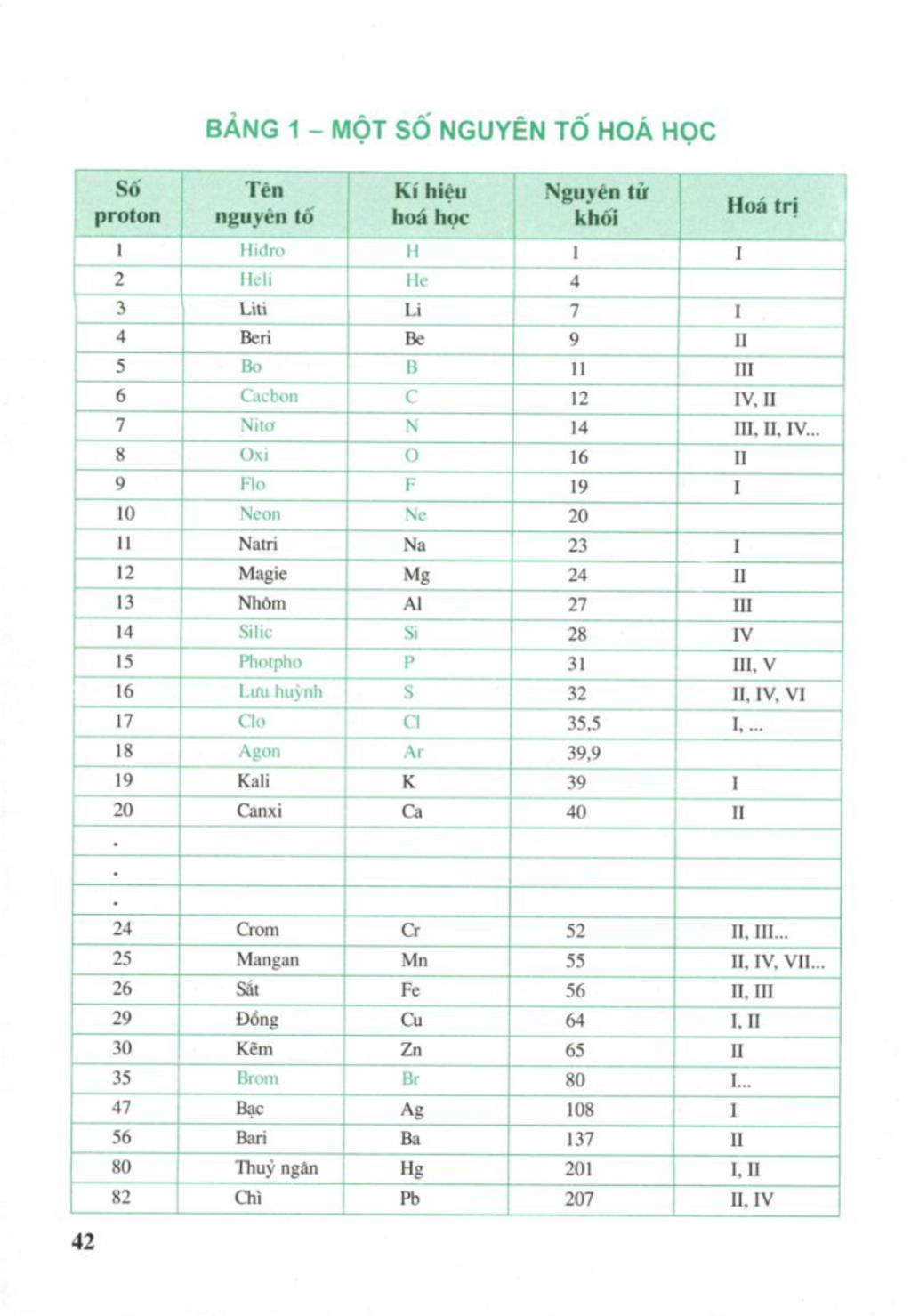
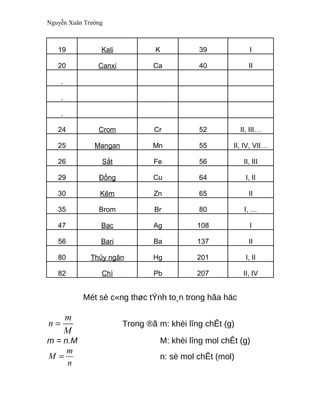
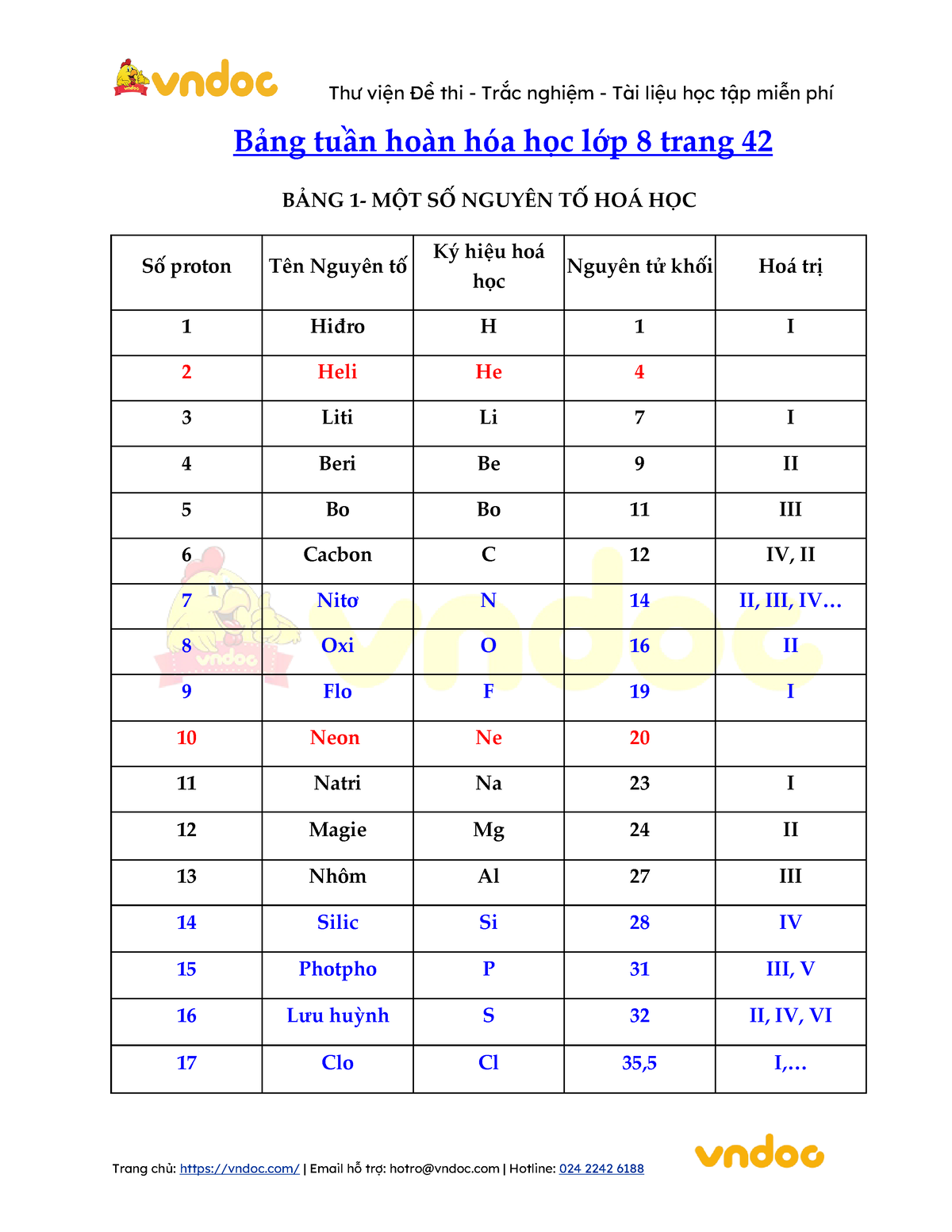
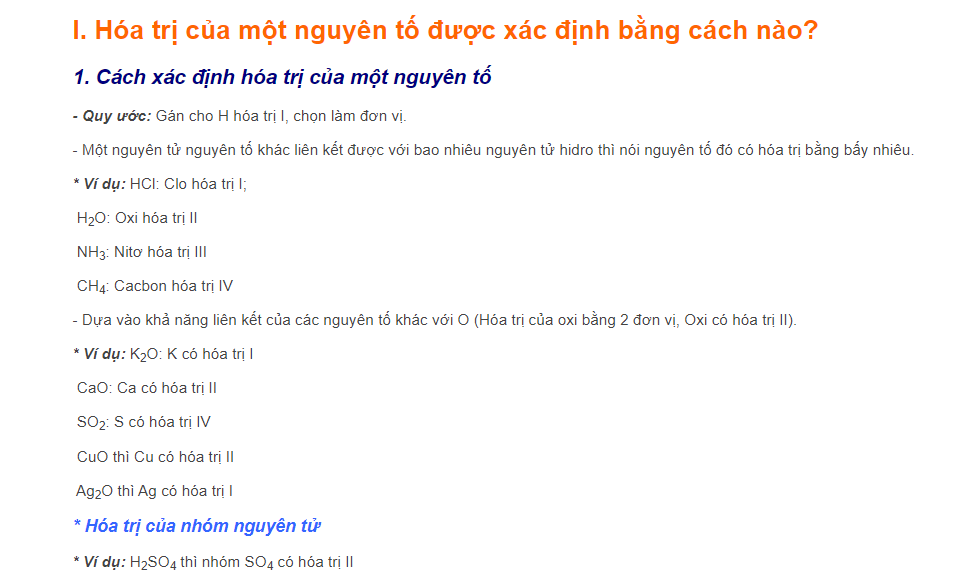
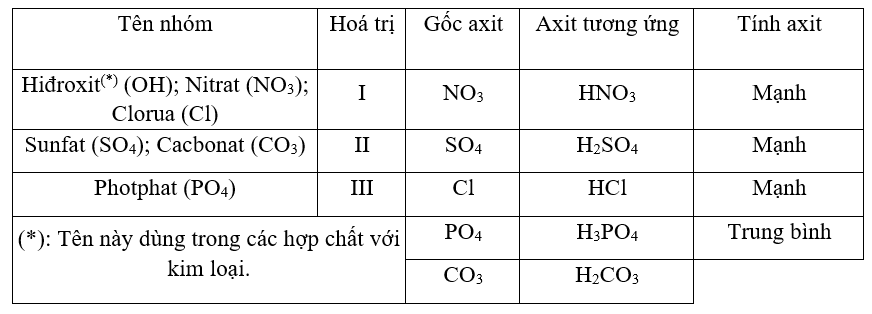
bảng hóa trị lớp 8
Cấu trúc của bảng hóa trị lớp 8:
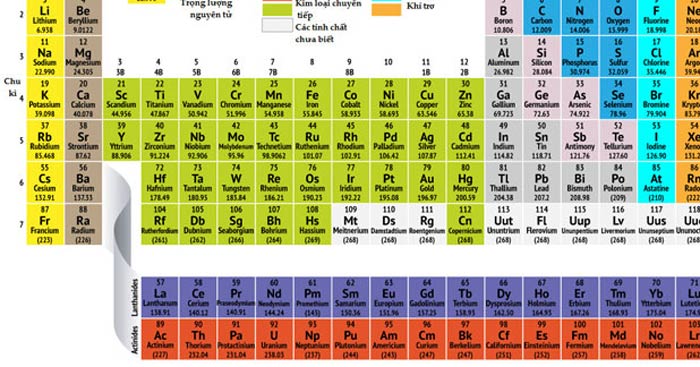
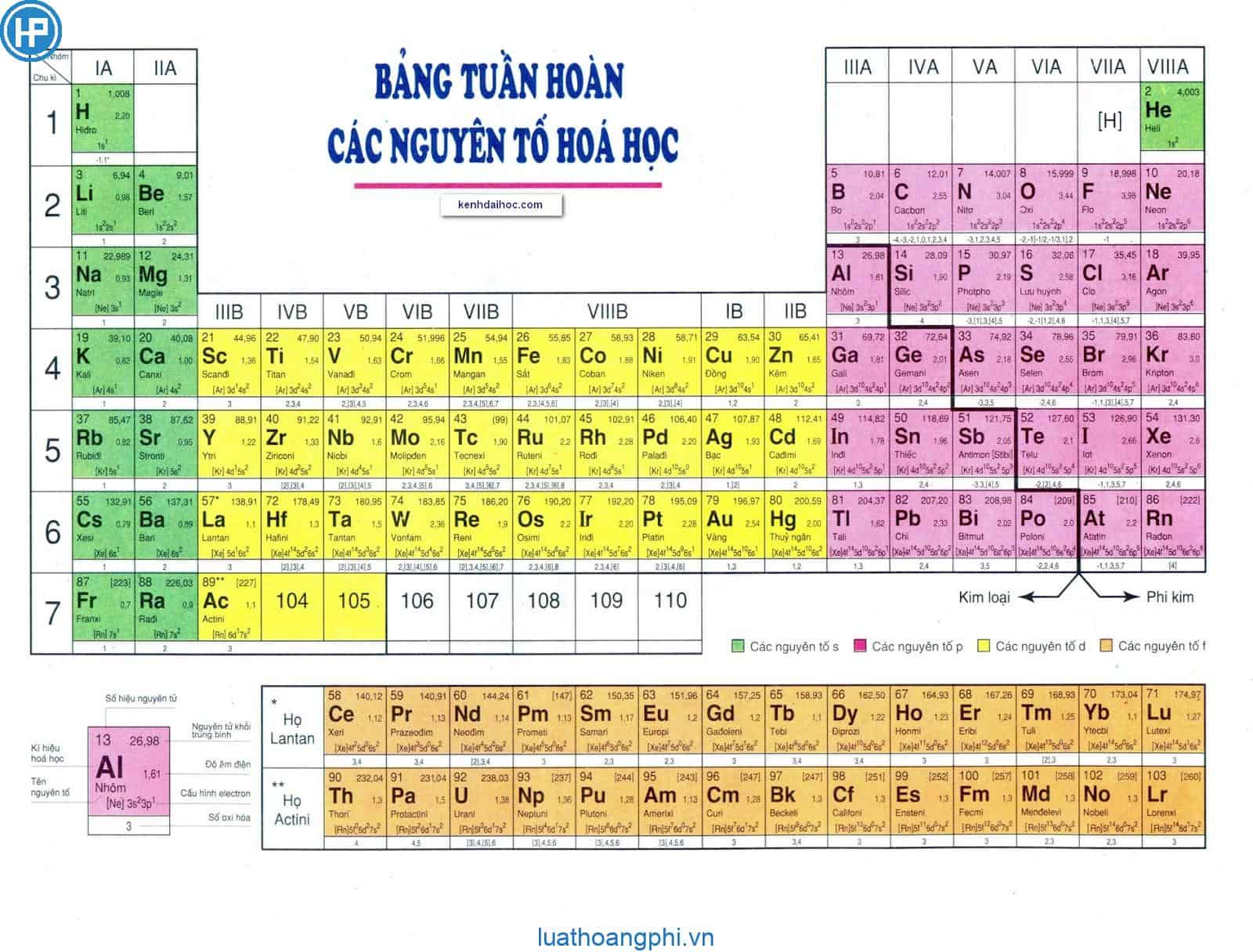
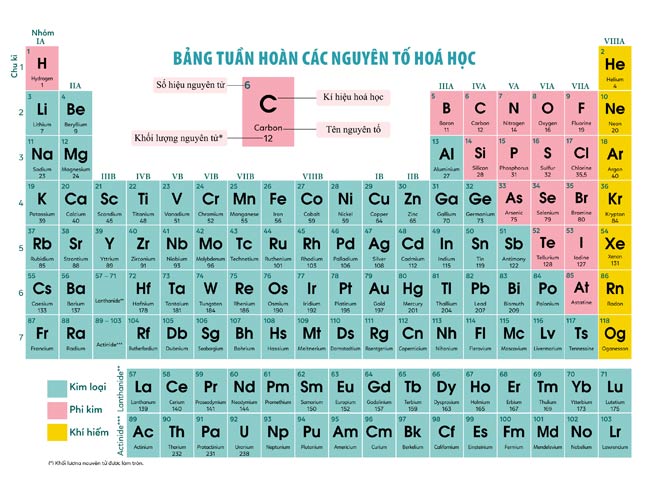
Bảng hóa trị lớp 8 được chia ra thành các nhóm tương ứng với số electron ngoài cùng của mỗi nguyên tố hóa học. Các nhóm này trong bảng hóa trị lớp 8 là những nhóm chính đó là nhóm IA đến nhóm VIIIA. Một cách tổng quát, các nhóm nằm bên trái bảng hóa trị có số lượng hóa trị bằng với số electron ngoài cùng của nguyên tố, còn các nhóm bên phải sẽ có số hóa trị bằng với 8 trừ đi số electron ngoài cùng. Một số đặc trưng của hai nhóm chính là nhóm s và nhóm p sẽ được trình bày trong các phần tiếp theo.
Các phần tử trong nhóm s:
Các phần tử trong nhóm s được đánh dấu từ nhóm IA đến nhóm IIA trong bảng hóa trị lớp 8. Tất cả các phần tử trong nhóm s đều có hai electron ngoài cùng, do đó chúng có số hóa trị bằng 2. Các phần tử này thường là kim loại và có xu hướng mất đi hai electron ngoài cùng để tạo ra ion dương. Ví dụ như natri (Na) trong nhóm IA sẽ tạo thành Na+, và magie (Mg) trong nhóm IIA sẽ tạo thành Mg2+.
Các phần tử trong nhóm p:
Các phần tử trong nhóm p được đánh dấu từ nhóm IIIA đến nhóm VIIIA trong bảng hóa trị lớp 8. Các phần tử trong nhóm p có từ ba đến bảy electron ngoài cùng, tương ứng với các nhóm từ IIIA đến VIIA. Chúng có số hóa trị bằng với số electron không ghép ion trong lớp electron bên ngoài. Các phần tử này có thể là kim loại (nhóm p1 đến nhóm p3) hoặc phi kim (nhóm p4 đến nhóm p7).
Cách đọc bảng hóa trị lớp 8:
Để đọc bảng hóa trị lớp 8, bạn cần xác định số lượng hạt nhân và electron của phần tử. Số hạt nhân bằng với số nguyên tử và được ghi ở trên cùng của ô tương ứng trên bảng. Số electron ngoài cùng bằng với số trên cùng ở bên phải của ô đó. Qui tắc xác định hóa trị của phần tử thường được dựa trên số electron không ghép ion trong lớp electron bên ngoài.
Ví dụ về cách đọc bảng hóa trị: Xét nguyên tố Decan (mã nguyên tử là X). X nằm trong nhóm VB và cách sử dụng bảng hóa trị để xác định hóa trị của X như sau:
– Số electron trong lớp electron bên ngoài của X = 5
– Do đó, hóa trị của X sẽ là 5 – 8 = -3
Các phản ứng hóa học dựa trên bảng hóa trị lớp 8:
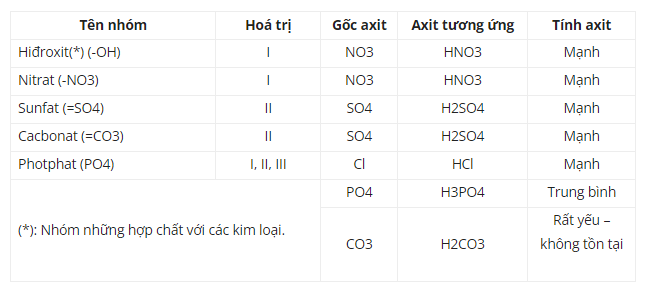
Các phản ứng hóa học dựa trên bảng hóa trị lớp 8 có thể được phân loại thành các loại phản ứng cơ bản, bao gồm phản ứng oxi hóa khử, phản ứng trao đổi ion, phản ứng đốt cháy, và phản ứng trao đổi khí. Cách sử dụng bảng hóa trị trong việc tính toán phần tử để sử dụng trong phản ứng hóa học được giải thích rõ ràng. Ví dụ: nếu muốn viết phương trình trao đổi ion giữa natri (Na) và axit clohidric (HCl), bạn cần biết rằng Na có hóa trị là +1 và Cl có hóa trị là -1
Ví dụ về các phản ứng hóa học dựa trên bảng hóa trị lớp 8: Một ví dụ về phản ứng oxi hóa khử dựa trên bảng hóa trị lớp 8 là phản ứng giữa magie và axit clohiđric để tạo thành muối clohiđrat và khí hiđro. Trong phản ứng này, magie có hóa trị là +2 và Cl ion có hóa trị là -1.
FAQs:
1. Có bao nhiêu nhóm trên bảng hóa trị lớp 8?
Trên bảng hóa trị lớp 8 có tám nhóm.
2. Tại sao các phần tử trong nhóm s có số hóa trị bằng hai?
Các phần tử trong nhóm s có hai electron ngoài cùng, do đó chúng có số hóa trị bằng 2.
3. Phản ứng hóa học nào được dựa trên bảng hóa trị?
Phản ứng hóa học có thể được dựa trên bảng hóa trị, bao gồm phản ứng oxi hóa khử, phản ứng trao đổi ion, phản ứng đốt cháy, và phản ứng trao đổi khí.
4. Làm thế nào để tính toán hóa trị của một phần tử?
Để tính toán hóa trị của một phần tử, bạn cần xác định số electron không ghép ion trong lớp electron bên ngoài.
5. Có bao nhiêu phân loại phản ứng hóa học cơ bản được dựa trên bảng hóa trị?
Có bốn phân loại phản ứng hóa học cơ bản được dựa trên bảng hóa trị.
Từ khoá người dùng tìm kiếm: bảng hóa trị lớp 8 Bảng hóa trị lớp 8 trang 42, Bảng hóa trị lớp 8 trang 43, Bảng hóa trị lớp 8 đầy đủ pdf, Bảng nguyên to hóa học lớp 8, Bảng nguyên to hóa học, Bảng hóa trị lớp 7, Bảng hóa trị lớp 9, Bảng nguyên tố hóa học lớp 7
Tag: Album 69 – bảng hóa trị lớp 8
[ HÓA HỌC 8-9] CÁCH NHỚ HÓA TRỊ NGUYÊN TỐ HÓA HỌC
Xem thêm tại đây: hienthao.com
Link bài viết: bảng hóa trị lớp 8.
Xem thêm thông tin về chủ đề bảng hóa trị lớp 8.
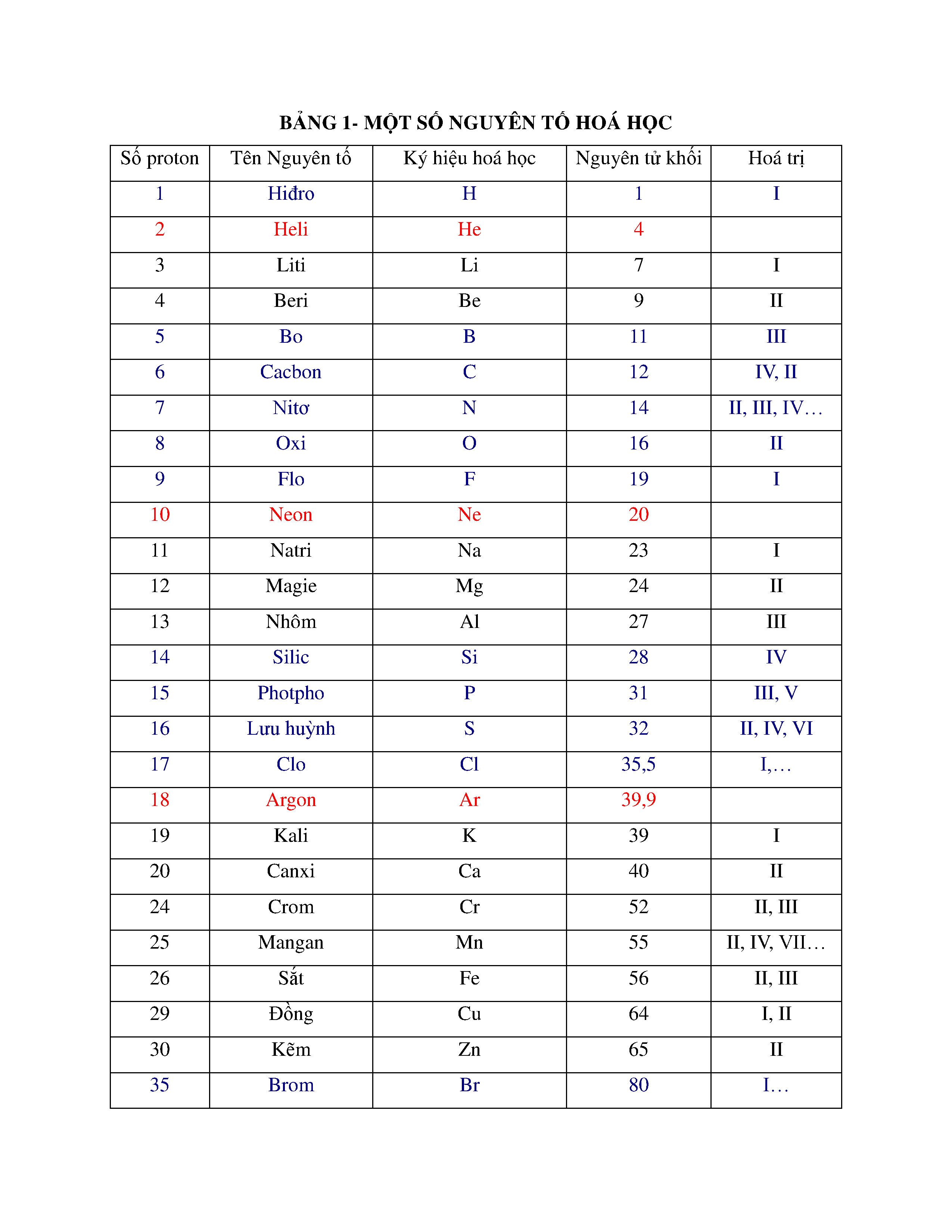
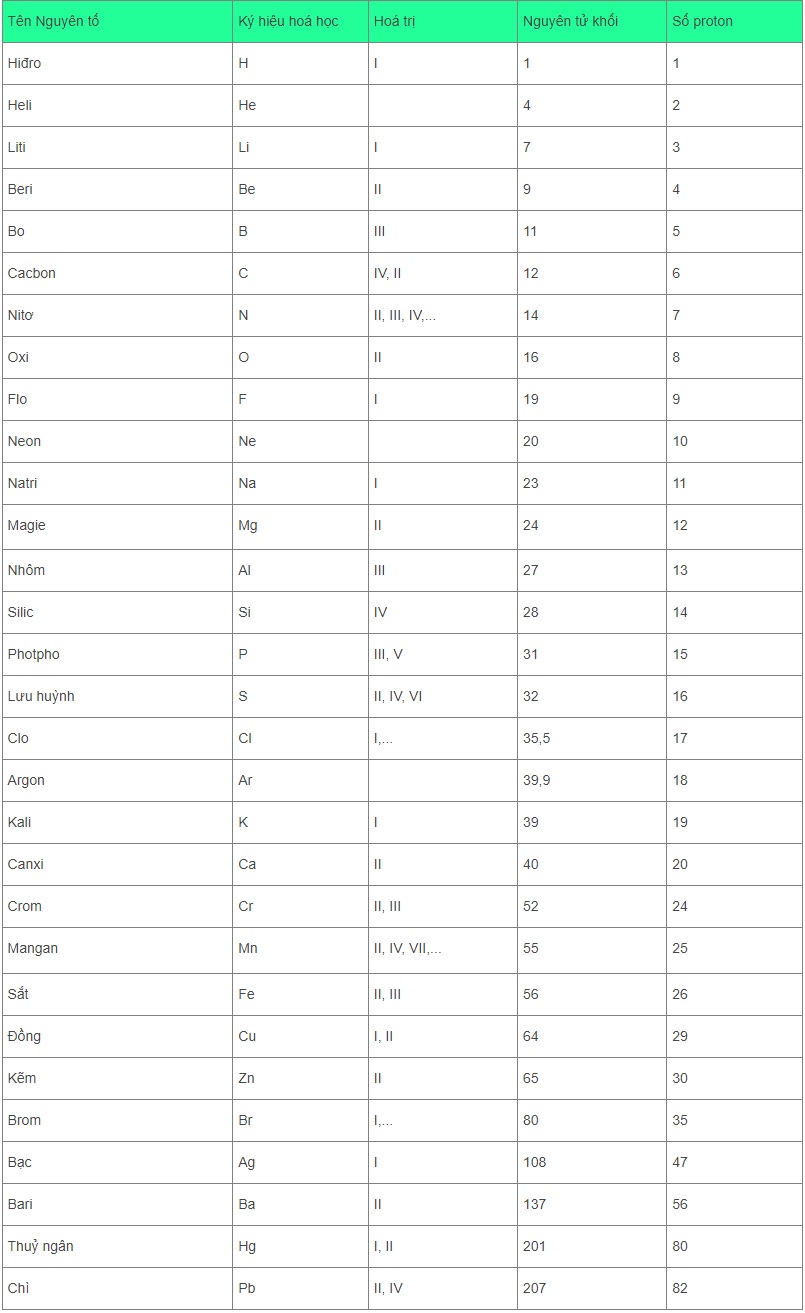
- Bảng hóa trị lớp 8 của một số nguyên tố hóa học thường gặp
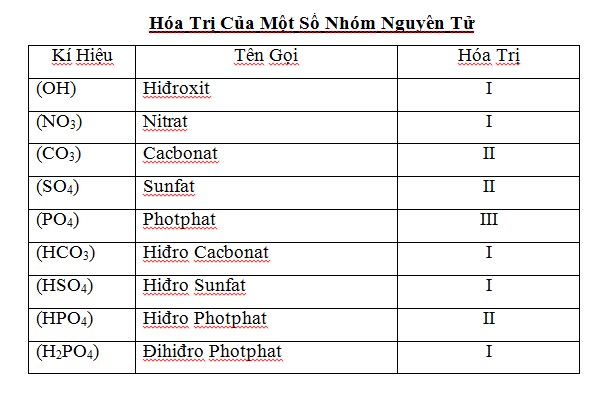
- Bảng Nguyên Tố Hóa Học Lớp 8 – Hóa trị của một số chất …
- Bảng hóa trị lớp 8 đầy đủ (Bảng hóa trị các nguyên tố …
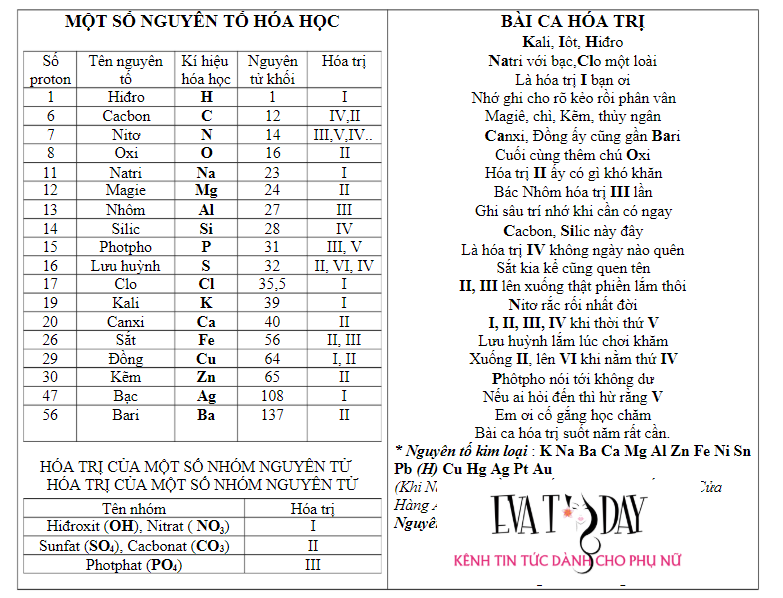
- Bảng Hóa Trị Lớp 8 Đầy Đủ ( Bài Ca Hóa Trị Chuẩn Nhất )
- Bảng hóa trị một số nguyên tố hóa học thường gặp
- Bảng hóa trị các nguyên tố hóa học lớp 8 trang 42-43 sgk
- Bang tuan hoan hoa hoc 8 trang 42 – Bảng tuần hoàn hóa …
- Bảng hóa trị lớp 8 – VnDoc.com
- bảng hóa trị lớp 8 trang 42 – 123doc
Categories: hienthao.com/category/tin-tuc
